هالوژنوآلکان ها که به نام هالوآلکان ها و آلکیل هالیدها نیز شناخته می شوند، ترکیبات آلی هستند که از آلکان ها به دست می آیند، اما یک هیدروژن جایگزین هالوژن می شود. آنها بخشی از یک دسته بسیار بزرگتر هستند که به نام هالوکربن ها شناخته می شوند. هیدروکربن هایی که بیش از یک هیدروژن با یک هالوژن جایگزین شده باشند نامیده می شوند هیدروکربن های هالوژنه.
هالوژنوآلکان ها کاربردهای تجاری و صنعتی متعددی دارد. به عنوان مثال، این ترکیبات معمولا در تولید شیمیایی به عنوان اجزای فعال در بازدارنده های شعله. برخی از هالوژنوآلکان ها نیز به عنوان مبرد و پیشران استفاده می شوند، در حالی که برخی دیگر در سنتز محصولات دارویی استفاده می شوند.
برخی از انواع هالوژنوآلکان ها به عنوان آلاینده اثرات زیست محیطی جدی دارند. اینها به تدریج حذف شده اند، مانند کلروفلوئوروکربن هایا CFC ها
هالوژنوآلکان ها چه دسته هایی هستند؟
هالوژنوآلکان ها به دو دسته تقسیم می شوند سه دسته: اولیه، ثانویه و سوم.
این دسته ها از تعداد گروه های آلکیل متصل به کربنی که جانشین هالوژن را حمل می کند، به دست می آیند.
کربن می تواند تا سه پیوند کووالانسی با سه گروه آلکیل دیگر و یک پیوند کووالانسی با اتم هالوژن تشکیل دهد.
- هالوژنوآلکان اولیه: جایی که تنها یک گروه آلکیل به کربنی که دارای جانشین هالوژن است متصل است.
- هالوژنوآلکان ثانویه: در این نوع دو گروه آلکیل با هالوژن به کربن متصل می شوند. آلکیل ها ممکن است از یک نوع یا انواع مختلف باشند.
- هالوژنوآلکان سوم: کربن حامل هالوژن دارای سه گروه آلکیل است که مستقیماً به آن متصل هستند. گروه های آلکیل یا از یک نوع هستند یا ترکیبی از انواع مختلف.
خواص هالوژنوآلکان ها چیست؟
هالوژنوآلکان ها بسیار مشابه هستند مشخصات فیزیکی به آلکان هایی که از آنها مشتق شده اند. درست مانند آلکان های اصلی خود، هالوآلکان ها بی رنگ، قابل اشتعال و برخی آبگریز هستند.
نقطه ذوب و جوش
نقطه ذوب و جوش برخی از هالوآلکان ها به طور قابل توجهی بالاتر از آلکان های اصلی آنها است. این به ویژه برای کسانی که دارای کلر، برم، و ید اتم های موجود در آنها، مشروط بر اینکه هالوژنوآلکان دارای اتم های کربن مشابه با آلکان اصلی باشد.
دلیل اصلی برای نقاط جوش بالاتر آنها وزن اتمی سنگینتر است که توسط اتمهای هالوژن به آلکانها اضافه میشود. در نیروهای بین مولکولی همچنین به دلیل قطبش پذیری بیشتر جزء هالوژن به طور قابل توجهی افزایش می یابد.
از طرفی نقطه جوش هالوآلکان ها به نسبت افزایش تعداد شاخه ها کاهش می یابد. هالوآلکان های ایزومر نقطه جوش کمتری نسبت به آلکان های مادر خود دارند. یک نمونه از این است 2-بروموپروپانکه نقطه جوش آن 72.85 درجه سانتیگراد است. آنالوگ آلکان آن، 1-بروموبوتان، دارای نقطه جوش 101.85 درجه سانتیگراد است.
اشتعال پذیری و قطبیت
مانند والدین آلکانی خود، هالوژنوآلکان ها قابل اشتعال هستند – اما نه به اندازه آلکان ها قابل اشتعال. هالوآلکان ها پیوندهای کربن-هیدروژن کمتری نسبت به آلکان ها دارند و اتم هالوژن هالوژنوآلکان ها را اندکی قطبی می کند. بنابراین، آنها به طور قابل توجهی به عنوان حلال در مقایسه با آلکان ها بهتر هستند. برخی از هالوژنوآلکان ها تا حدی در آب محلول هستند.
نیروهای بین مولکولی
قدرت نیروهای بین مولکولی، به ویژه نیروهای پراکندگی واندروالس، با طول مولکول های آلکان نسبت مستقیم دارد. با طولانی تر شدن زنجیره هالوژنوآلکان، نیروهای بین مولکولی قوی تر می شوند. زنجیره های طولانی تر برای شکستن به انرژی بیشتری نیاز دارند.
به طور مشابه، جاذبه های دوقطبی-دوقطبی واندروالس نیز با قطبی شدن مولکول ها به دلیل افزودن هالوژن افزایش می یابد. تنها استثنا ید است زیرا ارزش الکترونگاتیوی مشابه کربن دارد.
واکنش پذیری شیمیایی
در واکنش شیمیایی هالوژنوآلکان ها با پیوند بین گروه آلکیل و جانشین هالوژن رابطه معکوس دارد. هالوژنوآلکان هایی با پیوندهای ضعیف تر واکنش پذیرتر از هالوژنوآلکان هایی با پیوندهای قوی تر هستند. استحکام پیوند با الکترونگاتیوی هالوژن نسبت مستقیم دارد. این مقایسه است الکترونگاتیوی هالوژن ها مقادیر هالوژن ها:
- F (4.0)
- Cl (3.0)
- Br (2.8)
- من (2.5)
انواع واکنش هالوژنوآلکان ها چیست؟
واکنش هالوژنوآلکان ها با سایر ترکیبات و عناصر عمدتاً توسط جانشین هالوژن تعیین می شود. هالوآلکان ها دو نوع واکنش اصلی دارند: جایگزینی و حذف. این انواع اصلی همچنین دارای پنج زیر دسته از واکنش ها هستند:
- واکنش های جایگزینی: این واکنش ها شامل جایگزینی هالوژن با عنصر دیگری است. فرمول کلی واکنش های جانشینی را می توان به صورت زیر نوشت:
RX + Nu– → R-Nu + X–
- جایگزینی نوکلئوفیلیک: این واکنش زمانی رخ می دهد که یک ماده شیمیایی هسته دوست، یک جفت الکترون را به یک الکتروفیل اهدا کند. نوکلئوفیل جایگزین الکتروفیل در یک ترکیب می شود. هالوژن واکنش پذیرتر (نوکلئوفیل) جایگزین هالوژن کمتر واکنش پذیر می شود. به عنوان مثال، برم موجود در متیل بروماید را می توان به راحتی با کلر جایگزین کرد و متیل کلرید را تشکیل داد، همانطور که در تصویر زیر نشان داده شده است:
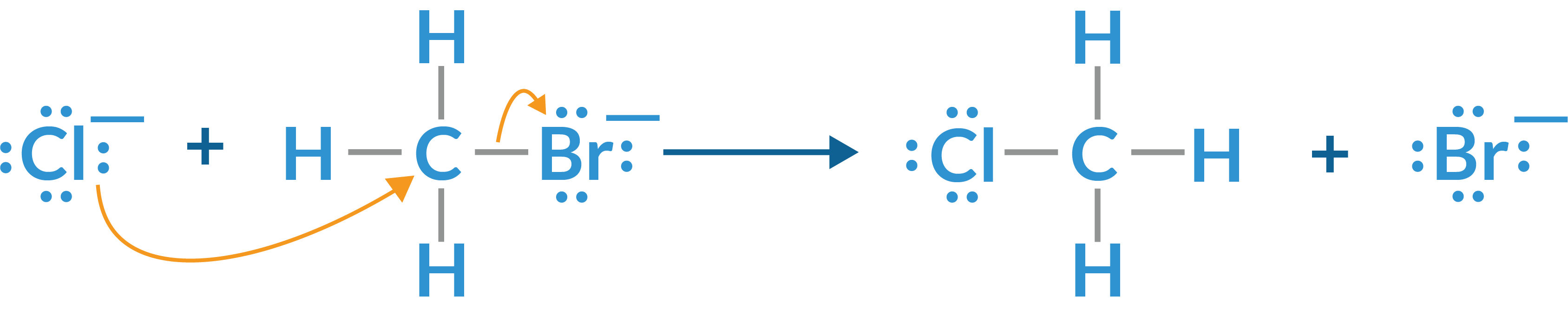
- جایگزینی الکتروفیلیک: این را می توان به عنوان مخالف جایگزینی هسته دوست در نظر گرفت. یک جایگزین آلکان یک هیدروژن را از یک ترکیب معدنی خارج می کند. یک جایگزین آلکان دارای کمبود الکترون است و ممکن است با گونه های هسته دوست، مانند هالیدهای هیدروژن، یون های نیترونیوم و تری اکسید گوگرد واکنش نشان دهد.
- جایگزینی رادیکال: رادیکال های آزاد در این نوع واکنش ها نقش دارند. رادیکال های هالوژن ممکن است با آلکان ها واکنش نشان دهند.
- واکنش های حذف / هیدروژن زدایی: در این نوع واکنش هالوژن و یک هیدروژن مجاور (پروتون) حذف می شوند. از این واکنش یک آلکن تشکیل می شود.
کاربرد هالوژنوآلکان ها چیست؟
هالوژنوآلکان ها کاربردهای تجاری و صنعتی متعددی دارند. قبلاً، بسیاری از این ترکیبات به عنوان مبرد و بازدارنده آتش استفاده می شدند، اما بعداً مشخص شد که تهدیدهای جدی زیست محیطی هستند. در اینجا برخی از کاربردهای دیگر هالوآلکان ها آورده شده است:
- محصولات دارویی: بسیاری از محصولات دارویی، از جمله برخی از مارک های دارویی برتر، دارای ترکیبات آلکیل فلوراید هستند. برخی از برندهای معروف عبارتند از بی حس کننده Rohypnol و ضد افسردگی Prozac.

- حلال های صنعتی: از این مواد برای حل کردن بسیاری از مواد و پردازش آنها به محصولات مختلف مانند تفلون استفاده می شود. به عنوان مثال می توان به کلروفرم، دی کلرومتان، دی کلرواتن و تری کلرواتان اشاره کرد.
- مواد بخور: آلکیل برومیدها عمدتاً به عنوان مواد بخور برای از بین بردن آفات مانند برخی از گونههای حشرات و نماتدها استفاده میشوند.
برای اطلاعات بیشتر در مورد منابع شیمی سطح A برای کمک به شما در بازنگری و برای اطلاعات در مورد مطالعه سطح A، ما را بررسی کنید مرکز منابع سطح شیمی.
